编者按:第52届ASCO年会正在紧锣密鼓地召开,会场每天公布的最近研究报告数以千计!美国费城宾夕法尼亚大学Noelle V. Frey等报告了应用优化嵌合抗原受体(CAR)-T细胞治疗复发/难治成人CD19+ 急性淋巴细胞白血病(ALL)的最新结果(大会摘要号:7002),引发现场关注。本刊特邀中国医学科学院血液病医院邱录贵教授就此项研究的结果和意义进行特约点评。
邱录贵 中国医学科学院血液病医院
CAR-T细胞治疗是近几年发展迅速的新的免疫治疗技术。与已知的抗体药物相比,CAR-T明显表现出对肿瘤细胞更强的靶向性和杀伤力。目前最成功的是针对CD19抗原的CAR-T治疗;临床试验结果显示,对难治/复发急性B-ALL的缓解率接近90%。由于新的抗体类药物如blinatumomab等在国内尚未上市,当前这项技术在国内发展迅猛,多家单位正在进行CAR-T治疗的临床研究。
该研究纳入27例ALL患者,中位年龄44(21~72)岁。其中,5例为原发耐药,9例接受过blinatumomab治疗,9例为异基因造血干细胞移植(allo-SCT)后复发患者。患者自体T细胞被体外导入慢病毒载体,使其编码鼠源抗CD19 scFv/4-1BB/CD3ζ (CTL019)CAR;患者在去除淋巴细胞治疗后输入CTL019。
患者根据输注剂量的不同被分为4个研究队列。在队列1、2中,9例患者输注5×107 CTL019(6例1次输入,3例分次输入),其中6例出现3/4级细胞因子释放综合征(CRS),托珠单抗治疗有效; 3例(33%)患者疾病获得完全缓解(CR)。队列3中,6例患者1次输入5×108 CTL019,其中3例死于CRS,对糖皮质激素和托珠单抗无效,血培养显示合并败血症;另3例患者获得CR。12例患者计划分次(10% d1, 30% d2 和60% d3)输入5×108 CTL019,若早期出现CRS症状则后续CTL019输注剂量调整,出现3级CRS时抗细胞因子治疗。队列4中,12例患者中9例发生可控的3/4级CRS;客观缓解率(ORR)为 83%(CR9例和PR1例)。
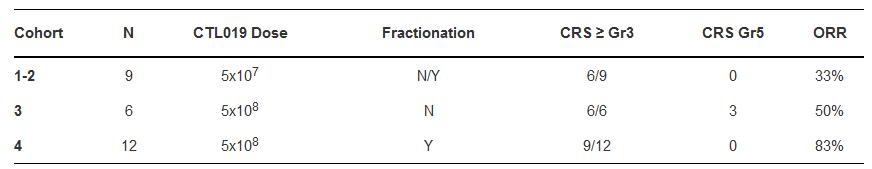
图1. CAR-T细胞治疗剂量、疗效及不良反应
CAR-T细胞治疗在显示出临床有效性的同时,也出现CRS、脱靶效应、神经系统毒性等临床毒副作用。如何控制这些不良反应、减少毒副作用,优化CAR-T治疗,也是该治疗中亟待关注和解决的问题。
细胞因子释放综合症(CRS)是目前为止CAR-T治疗过程中最严重的毒副作用。细胞因子是由激活的免疫细胞、以其与靶细胞相互作用而释放的。一定水平的细胞因子释放是免疫细胞疗效所必须的;然而一旦“过度”,对机体造成严重的损伤,甚至危及生命。理想的方法是优化所修饰的T-细胞的结构,使T-细胞在保留肿瘤杀伤活性的同时,让细胞因子的释放管控在一个安全的范围。如在CAR-T细胞上导入类似开关式装置,在需要激活免疫细胞的时候,利用生物或化学药物诱导免疫细胞的激活。或将自杀基因导入CAR-T细胞,当急性不良反应发生时启动自杀基因,诱导免疫细胞的凋亡。然而,这些尚处在实验研究阶段。
研究发现,监测INFγ、IL-6、和sgp-130等细胞因子水平是简单易行的危险预测方法。有效的预防性措施包括优化输注CAR-T细胞剂量、间隔,合理应用白介素6受体的抗体如托珠单抗(tocilizumab)和糖皮质激素等。上述该研究的结果证实,高剂量(5×108 )CTL019治疗难治/复发的成人B-ALL的疗效更佳;采用分次输入并根据早期CRS反应调整剂量不影响治疗的有效性,而改善了安全性。严重CRS并发败血症死亡风险高,因而预防感染和早期干预CRS是必要的。
另一方面,CAR-T治疗的时机也是影响疗效和毒性的重要因素。在本届ASCO年会上,来自美国纽约斯隆-凯特琳纪念癌症中心的Joe Hong Park等也报告了其I期临床试验结果(大会摘要号:7003)。复发/难治B-ALL患者46例,根据治疗前骨髓原始细胞计数分为2组:原始细胞<5%(MI,21例)和≥5%(MA,25例)。去除淋巴细胞治疗后输入19-28z CAR-T细胞。MI组91%和71%的患者获得CR和微小残留病阴性CR者(MRD-CR),而在MA组分别为75%和65%。严重CRS(44% vs. 0%)和3/4级神经毒性(40% vs. 14%)的发生率MA组显著高于MI组。中位随访12.0(1~45)个月,预期6个月OS率在MI和MA组分别为73%和57%;MI组12个月后尚无患者复发/死亡。获得MRD-CR者预期6个月OS率在MI组为92%,并且显示缓解持续超过3年;而MA组的OS率为65%。这项研究结果表明,19-28z CAR-T细胞治疗成人复发/难治B-ALL疗效显著;肿瘤细胞负荷小的患者治疗毒性低而长期生存更佳。支持19-28z CAR-T细胞治疗应用于ALL治疗的相对早期阶段如早期复发,甚至一线治疗时期。
总之,目前针对CD19的CAR-T细胞治疗获得了良好效果。深入了解其原因和机制,有助于我们提高CAR-T细胞治疗的疗效,同时有效控制治疗的不良反应,有效拓展该疗法的临床应用。
原文链接:Noelle V. Frey, Pamela A Shaw, Elizabeth O. Hexner, et al. Optimizing chimeric antigen receptor (CAR) T cell therapy for adult patients with relapsed or refractory (r/r) acute lymphoblastic leukemia (ALL). J Clin Oncol 34, 2016 (suppl; abstr 7002)
专家简介:
.jpg)
邱录贵,主任医师、博士生导师,中国医学科学院血液病医院(血液学研究所)现任医院淋巴瘤诊疗中心主任,中国抗癌协会血液肿瘤专业委员会候任主任委员、中国淋巴瘤研究联盟副主席、中华医学会血液学会委员(骨髓瘤工作组组长),主要从事恶性淋巴瘤、多发性骨髓瘤、急慢性淋巴细胞白血病等淋巴系统肿瘤的精确诊断及基于预后分层的整体治疗,在造血干细胞移植及淋巴系统肿瘤的临床和相关基础研究方面卓有建树,荣获天津市、教育部科技成果奖5项,在国内外重要专业杂志上发表论著250余篇,其中在包括NEJM、Lancet Oncology、Blood、Leukemia、Clinical Cancer Research和Haematologica等国际主流 SCI 杂志发表论文近60篇。





 京公网安备 11010502033352号
京公网安备 11010502033352号